Malattia di Pompe: nuove prospettive terapeutiche | La terapia...
La terapia enzimatica sostitutiva ha cambiato la prognosi dei...
La malattia di Pompe (MP) è una rara miopatia metabolica autosomica recessiva, causata dal deficit di alfa-glicosidasi acida lisosomiale (GAA), che determina accumulo di glicogeno in diversi tessuti e organi, particolarmente nel muscolo scheletrico, cardiaco e liscio. In base all’età di esordio della MP e alla gravità dei sintomi, sono riconosciute forme infantili (IOPD) e tardive (LOPD). Le forme infantili, se non trattate, sono fatali nella prima fase della vita, soprattutto quelle classiche con grave cardiomiopatia ipertrofica, mentre i fenotipi tardivi sviluppano disabilità motoria progressiva e necessità di supporto ventilatorio (1).
Strategie terapeutiche
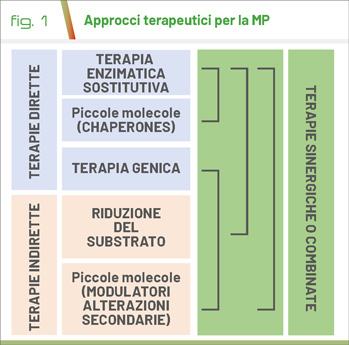 Gli approcci terapeutici proposti negli anni si basano su strategie che mirano alla correzione di diversi aspetti coinvolti nella cascata patogenetica della malattia (Fig. 1).
Gli approcci terapeutici proposti negli anni si basano su strategie che mirano alla correzione di diversi aspetti coinvolti nella cascata patogenetica della malattia (Fig. 1).
Le terapie dirette sono rivolte direttamente alla GAA. Puntano a ripristinare il difetto enzimatico primario e causativo della malattia:
- La terapia enzimatica sostitutiva (ERT) che prevede l’infusione periodica endovenosa della GAA ricombinante umana (rhGAA) in sostituzione dell'enzima difettoso. L’alglucosidasi è la prima ERT approvata per la MP (2); dopo oltre 20 anni ne sono chiari i benefici (sopravvivenza prolungata, miglioramento cardiologico e della debolezza muscolare e ridotta necessità di supporto ventilatorio), ma la risposta alla ERT è molto variabile tra diversi tessuti e tra pazienti (3,4). L’assorbimento di rhGAA ed il suo trasporto ai lisosomi sono mediati dal recettore del mannosio-6-fosfato (MPR). Le ERT di nuova generazione puntano a potenziare l’efficacia migliorando l’affinità della rhGAA con MPR in modo indipendente dalla glicosilazione (reveglucosidasi) o dipendente (avalglucosidasi e cipaglucosidasi), grazie alla presenza di un maggior numero di residui di mannosio-6-fosfato. Queste ultime due sono state approvate in seguito a trial clinici di fase III che ne hanno dimostrato la non-inferiorità in pazienti LOPD (5,6) e la migliore stabilizzazione di pazienti IOPD, rispetto alla terapia tradizionale (7).
- Le terapie con piccole molecole chaperones, che interagiscono direttamente con l’enzima migliorandone la struttura e la stabilità, possono agire sia sull’enzima difettoso endogeno che sull’enzima ricombinante (8).
- La terapia genica che prevede l’inserimento della copia normale del gene GAA (veicolata da un virus) che dirige la sintesi dell'enzima normale da parte delle cellule del ricevente. Studi preclinici sono stati condotti nel modello murino, utilizzando diversi approcci e protocolli terapeutici (9).
Le terapie indirette non agiscono direttamente sulla GAA, ma mirano a correggere aspetti correlati:
- La riduzione del substrato (SRT) riduce la quantità di glicogeno sintetizzata al fine di ripristinare l'equilibrio tra l'attività GAA difettosa e glicogeno che arriva ai lisosomi per essere degradato. L’inibizione della glicogeno-sintasi 1 muscolare può essere ottenuta con approcci di terapia genica con oligonucleotidi antisenso (10) o piccole molecole come MZ-101 (11).
- Gli approcci che agiscono sulle alterazioni cellulari secondarie al difetto enzimatico sono strategie completamente nuove. Esse mirano alla manipolazione e ripristino di alterazioni cellulari secondarie, come alterato flusso autofagico e/o aumentato stress ossidativo (12).
Terapie sinergiche o combinate
La combinazione di singoli approcci può potenziarne l’efficacia grazie ad un effetto sinergico e additivo. Sono stati proposti diversi approcci combinati. Alcuni esempi possono essere:
- La combinazione di ERT con piccole molecole chaperones; già proposta in studi preclinici e clinici con alglucosidasi e miglustat (13, 14) è alla base della nuova rhGAA cipaglucosidasi che va somministrata in associazione a miglustat.
- La combinazione di SRT con ERT; in modelli murini, è stata dimostrata la maggiore riduzione dell’accumulo di glicogeno muscolare, quando la ERT è somministrata in combinazione con MZ-101 (11).
- La combinazione di piccole molecole che agiscono su pathway secondari con ERT; modulatori di autofagia e stress ossidativo, in studi preclinici hanno dimostrato di migliorare l’efficacia della ERT e la riduzione del glicogeno (12). Tale combinazione può essere studiata anche per potenziare la terapia genica.
Problemi correlati da risolvere
La valutazione di pazienti trattati a lungo termine ha evidenziato un coinvolgimento neurologico progressivo, prima considerato assente o subclinico (15). Emerge dunque la necessità di raggiungere questo ulteriore target terapeutico con strategie in grado di superare la barriera emato-encefalica, come piccole molecole, ERT di fusione e terapie geniche con transgeni altamente secreti (16).
Parallelamente si è resa necessaria la disponibilità di biomarcatori adeguati e non invasivi per monitorare la risposta alle terapie e la progressione di malattia. Alcuni marcatori sono stati proposti e sono in corso studi per valutarne la potenziale affidabilità ed attendibilità nella pratica clinica (17).
Bibliografia
- Reuser AJ, Kroos MA, Hermans MM, et al. Glycogenosis type II (acid maltase deficiency). Muscle Nerve Suppl. 1995; 3:S61-9.
- Fukuda T, Roberts A, Plotz PH, et al. Acid alpha-glucosidase deficiency (Pompe disease). Curr Neurol Neurosci Rep. 2007; 7(1):71-7.
- Dornelles AD, Junges APP, Krug B, et al. Efficacy and safety of enzyme replacement therapy with alglucosidase alfa for the treatment of patients with infantile-onset Pompe disease: a systematic review and metanalysis. Front Pediatr. 2024; 12:1310317.
- Dornelles AD, Junges APP, Pereira TV, et al. A Systematic Review and Meta-Analysis of Enzyme Replacement Therapy in Late-Onset Pompe Disease. J Clin Med. 2021; 10(21):4828.
- Kishnani PS, Diaz-Manera J, Toscano A, et al. COMET Investigator Group. Efficacy and Safety of Avalglucosidase Alfa in Patients With Late-Onset Pompe Disease After 97 Weeks: A Phase 3 Randomized Clinical Trial. JAMA Neurol. 2023; 80(6):558-567.
- Schoser B, Roberts M, Byrne BJ, et al. PROPEL Study Group. Safety and efficacy of cipaglucosidase alfa plus miglustat versus alglucosidase alfa plus placebo in late-onset Pompe disease (PROPEL): an international, randomised, double-blind, parallel-group, phase 3 trial. Lancet Neurol. 2021; 20(12):1027-1037.
- Kishnani PS, Kronn D, Brassier A, et al. Mini-COMET Investigators. Safety and efficacy of avalglucosidase alfa in individuals with infantile-onset Pompe disease enrolled in the phase 2, open-label Mini-COMET study: The 6-month primary analysis report. Genet Med. 2023; 25(2):100328.
- Borie-Guichot M, Tran ML, Génisson Y, et al. Pharmacological Chaperone Therapy for Pompe Disease. Molecules. 2021; 26(23):7223.
- Unnisa Z, Yoon JK, Schindler JW, et al. Gene Therapy Developments for Pompe Disease. Biomedicines. 2022; 10(2):302.
- Weiss L, Carrer M, Shmara A, et al. Skeletal muscle effects of antisense oligonucleotides targeting glycogen synthase 1 in a mouse model of Pompe disease. bioRxiv [Preprint]. 2024 Mar 2:2024.02.22.580414.
- Ullman JC, Mellem KT, Xi Y, et al. Small-molecule inhibition of glycogen synthase 1 for the treatment of Pompe disease and other glycogen storage disorders. Sci Transl Med. 2024; 16(730):eadf1691.
- Tarallo A, Damiano C, Strollo S, et al. Correction of oxidative stress enhances enzyme replacement therapy in Pompe disease. EMBO Mol Med. 2021; 13(11):e14434.
- Porto C, Cardone M, Fontana F, et al. The pharmacological chaperone N-butyldeoxynojirimycin enhances enzyme replacement therapy in Pompe disease fibroblasts. Mol Ther. 2009; 17(6):964-71.
- Parenti G, Fecarotta S, la Marca G, et al. A chaperone enhances blood a-glucosidase activity in Pompe disease patients treated with enzyme replacement therapy. Mol Ther. 2014; 22(11):2004-12.
- van den Dorpel JJA, Mackenbach MJ, Dremmen MHG, et al. Long term survival in patients with classic infantile Pompe disease reveals a spectrum with progressive brain abnormalities and changes in cognitive functioning. J Inherit Metab Dis. 2024. doi: 10.1002/jimd.12736. Online ahead of print.
- Puzzo F, Colella P, Biferi MG, et al. Rescue of Pompe disease in mice by AAV-mediated liver delivery of secretable acid a-glucosidase. Sci Transl Med. 2017; 9(418):eaam6375.
- Tarallo A, Carissimo A, Gatto F, et al. microRNAs as biomarkers in Pompe disease. Genet Med. 2019; 21(3):591-600.





