Rachitismo ipofosfatemico X-linked: nuovi approcci terapeutici...
Il rachitismo ipofosfatemico X-linked è una patologia ereditaria...
Descriviamo il caso di un lattante di 5 mesi, giunto alla nostra attenzione per il riscontro di craniotabe alla visita di controllo eseguita presso il pediatra di famiglia. In anamnesi familiare si segnala madre con bassa statura e varismo agli arti inferiori. All’esame obiettivo si rileva: fontanella anteriore molto ampia, bozze frontali prominenti, peso corrispondente al 25° pc e lunghezza inferiore al 5° pc. Gli esami ematochimici effettuati evidenziano ipofosfatemia (2,1 mg/dl), ipovitaminosi D (24,6 ng/ml), aumento della fosfatasi alcalina (778 U/l) associati a calcemia e paratormone nella norma.
Alla luce del quadro descritto è stata richiesta l’indagine genetica CGH array che ha identificato una microdelezione nella regione cromosomica Xp22.11 contenente il gene PHEX, responsabile del rachitismo ipofosfatemico a trasmissione X-linked (XLH-R). Tale analisi, estesa alla madre, ha evidenziato la medesima alterazione. Pertanto, veniva posta diagnosi e prescritta terapia con sali di fosfato e metaboliti attivi della vitamina D in somministrazioni pluriquotidiane.
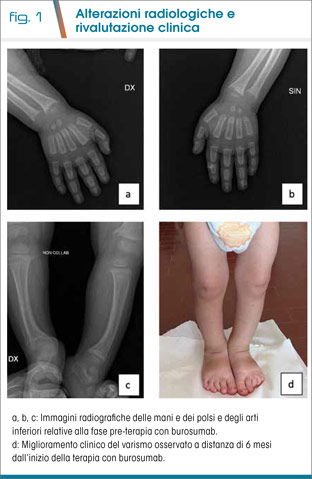 Al controllo clinico eseguito a distanza di circa un anno, il piccolo presentava ascessi periapicali nel cavo orale ed un atteggiamento varo degli arti inferiori; i parametri auxologici si attestavano al di sotto del 5° pc. Gli esami ematochimici eseguiti confermavano la persistenza delle alterazioni tipiche della patologia di base; alle radiografie degli arti superiori e inferiori si evidenziava malattia ossea (Fig. 1a, b, c), definita da un Rickets Severity Score>1.5, parametro quantitativo che consente di valutare la gravità del rachitismo sulla base dei segni radiografici. In relazione alla scarsa risposta clinico-laboratoristica alla terapia standard impostata come prima linea, si rendeva necessario considerare altre opzioni terapeutiche. Pertanto, valutata l’eleggibilità della terapia biologica sulla base del TmP/GFR (riassorbimento massimo del fosfato in relazione al filtrato glomerulare), dei parametri auxologici ed ematochimici del piccolo, veniva quindi intrapreso il trattamento con burosumab al dosaggio di 0,8 mg/kg in somministrazioni bisettimanali; le prime sei sono state effettuate presso il nostro centro, con successivo passaggio della terapia in regime domiciliare.
Al controllo clinico eseguito a distanza di circa un anno, il piccolo presentava ascessi periapicali nel cavo orale ed un atteggiamento varo degli arti inferiori; i parametri auxologici si attestavano al di sotto del 5° pc. Gli esami ematochimici eseguiti confermavano la persistenza delle alterazioni tipiche della patologia di base; alle radiografie degli arti superiori e inferiori si evidenziava malattia ossea (Fig. 1a, b, c), definita da un Rickets Severity Score>1.5, parametro quantitativo che consente di valutare la gravità del rachitismo sulla base dei segni radiografici. In relazione alla scarsa risposta clinico-laboratoristica alla terapia standard impostata come prima linea, si rendeva necessario considerare altre opzioni terapeutiche. Pertanto, valutata l’eleggibilità della terapia biologica sulla base del TmP/GFR (riassorbimento massimo del fosfato in relazione al filtrato glomerulare), dei parametri auxologici ed ematochimici del piccolo, veniva quindi intrapreso il trattamento con burosumab al dosaggio di 0,8 mg/kg in somministrazioni bisettimanali; le prime sei sono state effettuate presso il nostro centro, con successivo passaggio della terapia in regime domiciliare.
Recentemente è stata eseguita la rivalutazione clinica a distanza di sei mesi dall’inizio di tale trattamento, ed è stato osservato un aumento del fosfato sierico (3,1 mg/dl) e nel TmP/GFR, una riduzione parziale del varismo degli arti inferiori (Fig. 1d) e la risoluzione delle lesioni gengivali, in assenza di complicanze renali, quali nefrocalcinosi, che tipicamente insorgono in seguito al trattamento convenzionale.
Patogenesi
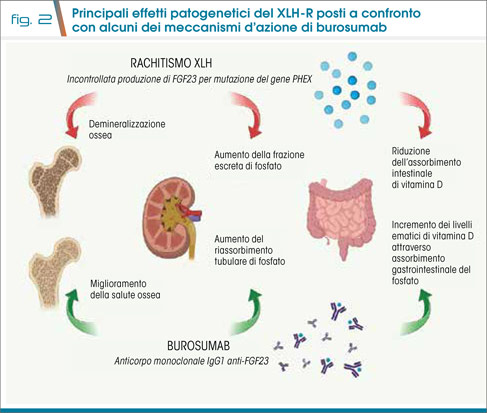 Il rachitismo ipofosfatemico X-linked è la forma più comune di rachitismo ereditario, causato da un’alterazione del gene PHEX, situato nella regione cromosomica Xp22.1, codificante per l’endopeptidasi che regola l’espressione del fattore di crescita dei fibroblasti 23 (FGF23). In presenza di una mutazione a carico di questo gene, si avranno alte concentrazioni di FGF23, che inibiscono il riassorbimento del fosfato a livello renale e agiscono sulla riduzione dei livelli ematici di vitamina D, attraverso due meccanismi d’azione: riducendo l’attività dell’enzima 1-alfa-idrossilasi, responsabile dell’idrossilazione della 25-OH-vitamina D in 1,25-OH2-vitamina D, ed aumentando il catabolismo della forma inattiva (Fig. 2).
Il rachitismo ipofosfatemico X-linked è la forma più comune di rachitismo ereditario, causato da un’alterazione del gene PHEX, situato nella regione cromosomica Xp22.1, codificante per l’endopeptidasi che regola l’espressione del fattore di crescita dei fibroblasti 23 (FGF23). In presenza di una mutazione a carico di questo gene, si avranno alte concentrazioni di FGF23, che inibiscono il riassorbimento del fosfato a livello renale e agiscono sulla riduzione dei livelli ematici di vitamina D, attraverso due meccanismi d’azione: riducendo l’attività dell’enzima 1-alfa-idrossilasi, responsabile dell’idrossilazione della 25-OH-vitamina D in 1,25-OH2-vitamina D, ed aumentando il catabolismo della forma inattiva (Fig. 2).
Manifestazioni cliniche
Il malfunzionamento del gene PHEX causa un accumulo dell’osteopontina, una sialoproteina nota come potente inibitore di mineralizzazione, che nei pazienti affetti da XLH-R impedisce la calcificazione ossea determinando osteomalacia e deformazioni soprattutto a carico delle ossa lunghe degli arti inferiori.
Ulteriori tipiche alterazioni associate alla patologia consistono in dismorfismi craniofaciali, dolori ossei, ritardo della crescita, alterazioni del cavo orale, quali ascessi gengivali, e disregolazione del metabolismo fosfo-calcico.
Terapia
Il trattamento di base prevede la somministrazione di sali di fosfato e metaboliti attivi della vitamina D, tuttavia, sebbene consenta di ridurre la gravità delle conseguenze legate all’eccesso di FGF23, non agisce direttamente sulla patogenesi.
Al fine di bloccare l’azione del FGF23 determinando un aumento del riassorbimento tubulare renale di fosfato e della concentrazione sierica di 1,25-OH2-vitamina D, è stato sviluppato burosumab, un anticorpo monoclonale umanizzato che lega tale molecola e che è stato approvato dalla Food and Drug Administration (FDA) nel 2018 e dall’Agenzia Italiana del Farmaco (AIFA) nell’anno successivo, per il trattamento dell'XLH-R in età pediatrica, nei bambini aventi almeno un anno di vita.
Conclusioni
XLH-R è una patologia ereditaria che comporta alterazioni scheletriche e del metabolismo fosfo-calcico. Burosumab offre notevoli vantaggi rispetto alla terapia convenzionale per il trattamento di tale patologia. Pertanto, risulta indispensabile una diagnosi precoce per avviare tempestivamente la terapia ed evitare complicanze a lungo termine.
Bibliografia
- Imel EA, Burosumab for Pediatric X-Linked Hypophosphatemia, Curr Osteoporos Re 2021; 19 (3);271–277.
- Lyseng-Williamson KA, Burosumab in X-linked hypophosphatemia: a profile of its use in the USA, Drugs Ther Perspect, 2018; 34(11): 497–506
- Fukumoto S,FGF23-related hypophosphatemic rickets/osteomalacia: diagnosis and new treatment. J Mol Endocrinol.2021; 66: (2) R57–R65.
- Baroncelli GI S. Mora S,X-Linked Hypophosphatemic Rickets: Multisystemic Disorder in Children Requiring Multidisciplinary Managemen, Front Endocrinol (Lausanne), 2021; 12: 688309.
- Rothenbuhler A, Schnabel D, Högler W, ALinglart A, Diagnosis, treatment-monitoring and follow-up of children and adolescents with X-linked hypophosphatemia (XLH), Metabolism 2020; 103S, :153892.





